服务热线
15150888188
问题1:欧洲药典Water in Bulk与Water in Container有何区别?
从使用角度分类,制药用水主要分为散装水(Water in Bulk)与包装水(Water in Container)两大类。散装水也称原料水,特指制药生产工艺过程中使用的水,例如,中国药典认可的散装水包括纯化水和注射用水;欧盟药典认可的散装水包括纯化水、高纯水和注射用水;美国药典认可的散装水包括纯化水、血液透析用水和注射用水等。包装水也称产品水,特指按制药工艺生产的包装成品水,例如,中国药典收录了灭菌注射用水;欧盟药典收录了包装纯化水和灭菌注射用水等;美国药典收录了抑菌注射用水、灭菌吸入用水、灭菌注射用水、灭菌冲洗用水和灭菌纯化水等多种产品水(表1)。
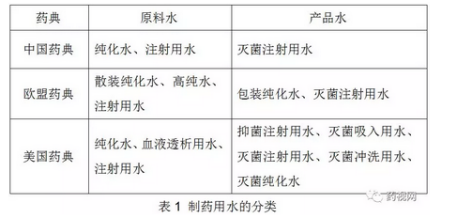
例如,美国药典灭菌纯化水是指包装并灭菌的纯化水,主要用于非肠道给药制剂以外的制剂配料。美国药典灭菌纯化水还可用于分析应用领域,当纯化水系统无法得到验证、纯化水用量很少、需要用灭菌纯化水或者包装的原料纯化水中微生物限度不符合要求时,可采用灭菌纯化水。
与欧盟药典不同,中国药典并没有区分散装水(Water in Bulk)与包装水(Water in Container),因此,中国药典2015版检测指标相对较多。

问题2:欧洲药典与美国药典注射用水质量标准为什么不需要检测重金属含量?
1. 美国药典认为,饮用水是纯化水或注射用水的原水,重金属项目不需要重复检测,饮用水国家标准会管控。
USP39-1231制药用水章节认为:“重金属检查的替代方法没有必要,因为①原水标准(国家初级饮用水条例)中对各 个重金属的规定,严于USP22 注射用水和纯化水重金属检查的近似数限度(约 0.1ppm); ②现代水系统的结构材料不会释放重金属污染物;③这一项检查结果为阴性——没有见 过重金属单项不合格的(即重金属检查不合格,而其他检查项合格),因为现行的饮用 水标准已经有重金属检查项。
中国药典纯化水保留重金属、亚硝酸盐、不挥发物等几个重要化学项目,很大程度是为了来共同保证电导率达到5.1us/cm@25℃时的纯化水还能满足使用要求。目前,欧盟药典已经确认纯化水标准参考美国药典纯化水标准是1.3us/cm@25℃.
2. 美国药典委员会认为关于重金属一项原有测定方法的灵敏度仅为mg/L级,而美国饮用水标准中一些金属离子的限度为μg/L级,远比USP规定严格。
中国药典的重金属检查法是指在实验条件下能够与硫代乙酞胺反应生成沉淀的金属杂质。如Ag, Pb, Hg,Cu, Cd, Bi, Zn, Co, Ni等,其中铅Pb***常遇到,且易积蓄中毒,因此,检查时以Pb为代表。对比中国饮用水和美国饮用水的标准,发现中国饮用水标准中对各个重金属的规定,也都基本上严于中国药典注射用水和纯化水重金属检查的近似数限度(约 0.1ppm)。
3.欧洲药典5.0版注射水有重金属检查项目,但是5.0以后删除了重金属项目。EP纯化水一直有重金属检查项目,但是规定“如果散装纯化水符合散装注射用水(0169)的电导率的规定,则不需要进行重金属检测。这也说明欧洲药典认可如果制药用水的电导率符合1.3us/cm要求,那么重金属项目不会不合格,可以不用检测。
4.国外《制药技术》2005年1月文章《USP电导率和EP重金属项目的对比》结果表明:USP电导率可以确定水样中是否含有重金属,且USP的电导率检测灵敏度高于EP的重金属检测方法,电导率测试可以替代重金属项目。数据结果见下图
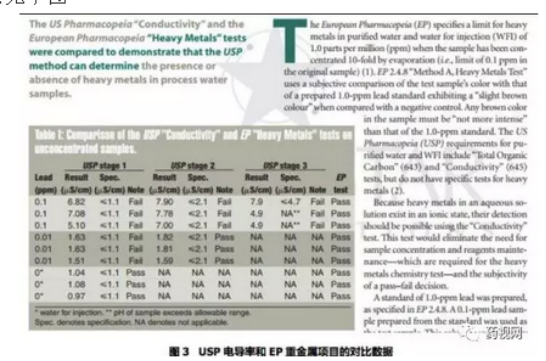
0.01ppm的标准铅溶液的电导率为1.63us/cm;0.1ppm的标准铅溶液的电导率为6.82us/cm,无法通过USP的电导率检测要求,但是却能通过EP的重金属检测,说明USP的电导率检测灵敏度高于EP的重金属检测方法。
这里有个问题:重金属在水中是否完全以离子形式存在?实验表明,在低浓度下,重金属在水中是完全解离的。
(1)因为目前中国药典的现有方法是硫代乙酰胺在弱酸性条件下水解,产生硫化氢,与重金属离子生成黄色到棕黑色的硫化物混悬液,与一定量标准铅溶液经同法处理后所呈颜色比较。若不是完全解离,则会有部分重金属无法被检出。
(2)可以从溶解度进行解释。查阅得知,PbSO4的溶解度为0.0041g/100g水(20℃),换算一下就是41ppm,远远大于药典规定的标准0.1ppm。同理,Pb(NO3)2在水中溶解度为56.5g/100g水。
5.回顾某公司近2年年终回顾数据和5年验证数据,显示电导合格,重金属项目没有不合格过。且某公司自己的研究实验也表明如果制药用水的电导符合1.3us的标准,那么重金属项目不会不合格。
实验过程见下方:
(1)将1000ppm的标准氨溶液稀释成100ppm、10ppm、1ppm、0.2ppm、0.02ppm、0.002ppm的梯度,并测电导率。
(2)将100ppm的标准铅溶液稀释成10ppm、1ppm、0.1ppm、0.01ppm、0.001ppm的梯度,并测电导率。
得到的数据如下:
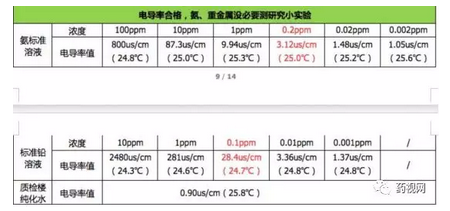
可以看到:
(1)当氨浓度为0.2ppm时,电导率为3.12us/cm;所以如果电导率不超过1.3 us/cm时,溶液中氨的浓度肯定不会超过0.2ppm。
(2)当铅浓度为0.1ppm时,电导率为28.4us/cm;所以如果电导率不超过1.3 us/cm时,溶液中铅的浓度肯定不会超过0.1ppm。
6.《中国药典分析检测技术指南》2017年07月第1版***提到电导率可以替代氨和重金属项目。这里的替代,应该意思可以直接用电导率项目来替代氨和重金属项目。把氨和重金属删掉。可以用电导率来定义水的化学纯度,因为电导率代表的是水中总离子数,而氨和重金属在水中又是以离子形式存在。
结论:目前,不仅有法规支持、文献资料支持、研究实验都表明,将水的电导率控制在≤1.3μS/cm (25℃)时,可以不测试重金属,因为此时重金属的浓度都肯定不会超过药典规定的限度。故中国药典的注射用水在有电导率检测的情况下,建议可以不用做重金属项目。
问题3:美国药典USP24关于制药用水指标到底发生了什么质的变化?
1996年11月15日,美国药典鼓励在线监测技术的应用,正式采用电导率仪测试法取代原有的微量离子浓度分析法,同时增加微生物含量检测要求,形成以电导率、TOC、微生物限度与内毒素含量为主的质量控制标准。表1为美国药典关于制药用水检测指标的变化过程。
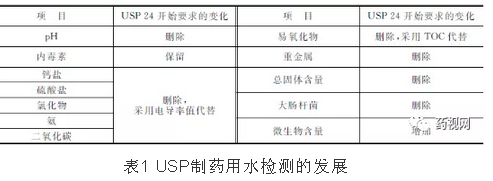
问题4:高温注射用水循环是GMP强制规定的吗?
WHO GMP:储存与分配系统需要设计良好的消毒或杀菌方式,以便有效控制生物荷载。水温***好控制在70~80摄氏度为宜,同时,15~20摄氏度也是认可的。
EU GMP:水处理设施及其分配系统的设计、安装和维护应能确保供水达到适当的质量标准;水系统的运行不应超越其设计能力;注射用水的生产、储存和分配方式应能防止微生物生长,例如,在70℃以上保温循环。
SFDA GMP:纯化水、注射用水的制备、储存和分配应当能够防止微生物的滋生。纯化水可采用循环,注射用水可采用70℃以上保温循环。
所有国家或地区的GMP法规都是强调“注射用水的生产、储存和分配方式应能防止微生物生长”,推荐采用70度以上保温循环模式,但并非强制。例如,在美国,大约有20%左右的生物制品企业采用常温或低温设计的注射用水系统进行药品生产。
问题5:制药用水水质质量控制中***核心的两个预防是什么?
以“质量源于设计”理念为基础的,预防颗粒物污染,预防微生物污染。