服务热线
15150888188
问题6:饮用水与自来水,是一回事吗?
自来水与饮用水是两个不一样的术语与概念。
自来水:是指通过自来水处理厂净化、消毒后生产出来的符合相应标准的供人们生活、生产使用的水。生活用水主要通过水厂的取水泵站汲取江河湖泊及地下水,地表水,由自来水厂按照《国家生活饮用水相关卫生标准》,经过沉淀、消毒、过滤等工艺流程的处理,***后通过配水泵站输送到各个用户。自来水在中国大陆一般不被用来直接饮用,但在世界某些地区由于采用了较高的质量管理标准而直接饮用。
饮用水:是指供人生活的饮水和生活用水。饮用水包括干净的天然泉水、井水、河水和湖水,也包括经过处理的矿泉水、纯净水等。加工过的饮用水有瓶装水、桶装水、管道直饮水等形式。2007年7月1日,卫生部和国家标准化管理委员会联合发布新的《生活饮用水卫生标准》(GB 5749-2006),该标准具有三个特点:加强了对水质有机物、微生物和水质消毒等方面的要求,该标准中的饮用水水质指标由原标准(GB 5749-85)的35项增至106项;统一了城镇和农村饮用水卫生标准;参考了世界卫生组织的《饮用水水质准则》,实现饮用水标准与国际接轨。由于中国地域广阔,各地具体情况不同,新标准中的水质全部指标***迟于2010年7月1日实施。中国《药品生产质量管理规范》(2010版)第99条规定:药品生产用水应适合其用途,应至少采用饮用水作为制药用水原料水。
自来水与饮用水是两个概念。制药行业中,***低级别的制药用水为饮用水,基于国情考虑,大多数企业只能采用自来水为制药用水的原水。如果自来水水质不符合饮用水标准,制药企业需将自来水引入制水间进行净化处理,遵照中国GMP规定,自来水不允许直接用于制药生产环节(包括洗手、洁具清洗)。原则上来讲,饮用水工程为国家工程,自来水企业有责任输送符合国家标准的饮用水到各个制药企业的制水间,饮用水水质判断标准不能***于自来水企业的设备出口,应该延伸到各个用水点用户处。
这个责任误区主要是市政管网无法时刻输送给企业符合GB的饮用水,导致企业需要自行进行净化处理,在自行净化自来水的过程中,产生了一系列将预处理列入纯化水机的“中国特色”的误区。
问题7:以饮用水为水源,经过蒸馏法制备的注射用水内毒素水平在什么级别?
注射用水的内毒素药典标准为不高于0.25EU/ml,饮用水中的内毒素含量水平大概在10-100EU/ml水平,饮用水经纯化水机净化后,其内毒素水平大概会在1-10EU/ml水平,相当于传统预处理+RO/EDI的纯化水机的内毒素去除能力为1-2log水平。蒸馏法分为三种:单效蒸馏、多效蒸馏与热压蒸馏,目前,单效蒸馏水机因不节能等原因,已被淘汰。工业化生产的制药企业普遍采用的是多效蒸馏水机与热压蒸馏水机。扬州亚飞主要生产的是多效蒸馏水机,采用降膜式外加三级分离技术,是目前国内制药行业的***。
通常情况下,热压蒸馏水机的内毒素去除能力大概在2-3log水平,也就是说,采用饮用水直接制备注射用水时具有一定的风险性,但采用纯化水经热压蒸馏水机制备注射用水时,内毒素含量低于0.1EU/ml,中国药典规定:注射用水需采用纯化水经蒸馏制备而得,因此,企业采用热压式蒸馏水机在中国制药企业使用是完全安全的。
多效蒸馏水机因设计不同,内毒素去除能力不尽相同,例如,采用升膜法设计的多效蒸馏水机,内毒素去除能力大概在2-3log水平;采用降膜法+外螺旋分离设计的多效蒸馏水机,内毒素去除能力***高可以达到3-4log水平。美国药典允许注射用水采用饮用水经蒸馏制备而得,主要是基于部分多效蒸馏水机具有3-4log的内毒素去除能力,饮用水为原水时,也能得到内毒素含量低于0.01EU/ml的注射用水。
扬州亚飞主要生产的是多效蒸馏水机,采用降膜式外加三级分离技术,是目前国内制药行业的***。
问题8:纯蒸汽与工艺蒸汽的区别是什么?
蒸汽在制药企业中是一种重要的公共工程,主要为制药用水的制备、工艺设备的温度控制提供热源,用于无菌工艺设备、器具、***终灭菌产品的灭菌等。蒸汽可大致分为工业蒸汽(Plant Steam或Black Steam)、工艺蒸汽(Process Steam)和纯蒸汽(Pure Steam或Clean Steam)。
工业蒸汽主要用于非直接接触产品的加热,为非直接影响系统,又可细分为普通工业蒸汽和无化学添加蒸汽。普通工业蒸汽是指由市政用水软化后制备的蒸汽,属于非直接影响系统,用于非直接接触产品工艺的加热,一般只要考虑系统如何防止腐蚀;无化学添加蒸汽是指由纯化过的市政用水添加絮凝剂后制备的蒸汽,属于非直接影响系统,主要用于空气加湿,非直接接触产品的加热,非直接接触产品工艺设备的灭菌,废料废液的灭活等。无化学添加蒸汽中不应该含有氨、肼等挥发性化合物。
工艺蒸汽属于直接影响系统,主要用于***终灭菌产品的加热和灭菌,冷凝液***少应该满足城市饮用水的标准。
纯蒸汽属于直接影响系统,经蒸馏方法制备而成,冷凝液需满足注射用水的要求。纯蒸汽用于湿热灭菌工艺时,还需在不凝性气体、过热度和干燥度方面达到EN285和HTM2010等标准的要求。纯蒸汽是由原水制备,所使用的原水是经过处理并至少满足饮用水要求,不少企业会采用纯化水或注射用水制备纯蒸汽,纯蒸汽不含挥发性添加剂,因此不会受到胺类或肼类杂质的污染,这对于预防注射剂产品的污染是极其重要的。
在蒸汽系统设计过程中采用哪种质量标准的蒸汽,可参考ISPE推荐的决策树,如下图所示。
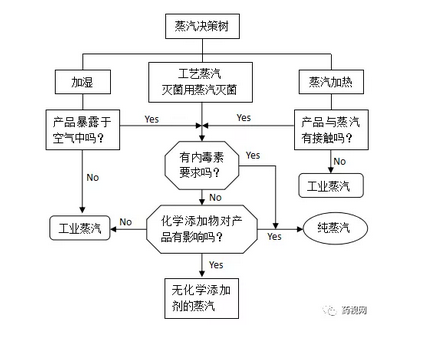
问题9:采用饮用水为源水,通过传统预处理+RO/EDI的纯化水机工艺,纯化水内毒素水平在什么级别?
注射用水的内毒素药典标准为不高于0.25EU/ml,饮用水中的内毒素含量水平大概在10-100EU/ml水平,饮用水经纯化水机净化后,其内毒素水平大概会在0.1-1EU/ml水平,相当于传统预处理+RO/EDI的纯化水机的内毒素去除能力为2-3log水平。实际上,国外有些企业,直接用饮用水+预处理+RO/EDI实现注射用水的制备。
问题10:肠道吸收与非肠道吸收对于制药用水的本质区别是什么?
肠道吸收药物因为通过了肠道的“过滤”作用,对制药用水中的内毒素指标没有要求;非肠道吸收药物,例如注射剂,因为没有经过肠道“过滤”,对制药用水中的内毒素指标往往具有很高的要求,否则容易引起热原反应。这也是纯化水与注射用水水质指标中一个非常明显的差异。需要注意的是:肠道吸收时,不允许有大肠杆菌的污染,这也是饮用水指标中明确“大肠杆菌不可见”的主要原因。
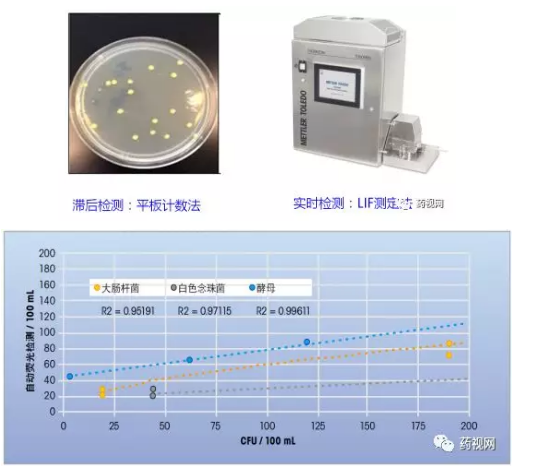
问题11:在线微生物限度检测仪器对传统平板计数法带来了哪些***性的冲击?
与TOC检测法颠覆易氧化物检测法类似,“激光诱导荧光光谱(LIF)测量技术”颠覆了“平板计数法”,它科学地解决了“大多数微生物是无法培养成菌落数的”这一客观存在的现实问题,因此,在线微生物检测技术将很可能带来世界范围内微生物限度检测标准的重新制定。
建立以“激光诱导荧光光谱(LIF)测量技术”为背景的微生物限度标准及PQ执行措施,是一个全新的课题。它将不仅是对中国制药行业的挑战,也是对包括美国在内的全世界范围内制药用水微生物检测技术与标准的挑战。
与在线TOC检测技术类似,激光诱导荧光光谱(LIF)测量的实时微生物检测技术将在接下来的10年会直接推动具有微生物检测需求的的行业,例如半导体或电子行业,但制药行业因为对微生物的检测实时性需求并不是***紧迫需求,制药用水药典指标检测方法的更新相对较慢,但相信未来还是会带来很大的变革的,比较PAT技术是主导发展方向。